Протеинкиназы
Протеинкина́зы — подкласс ферментов киназ (фосфотрансфераз). Протеинкиназы модифицируют другие белки путём фосфорилирования остатков аминокислот, имеющих гидроксильные группы (серин, треонин и тирозин) или гетероциклической аминогруппы гистидина.
Фосфорилирование, как правило, изменяет или модифицирует функции субстрата, при этом может изменяться ферментативная активность, положение белка в клетке, или взаимодействие с другими белками. Полагают, что до 30 % всех белков в клетках животных могут быть модифицированы протеинкиназами. В клетке протеинкиназы регулируют метаболические пути, а также пути сигнальной трансдукции и передачи сигналов внутри клетки.
Геном человека содержит около пятисот генов протеинкиназ, которые составляют около двух процентов всех генов.[1]
Химическая активность протеинкиназ заключается в отщеплении фосфатной группы от АТФ и ковалентном присоединении её к остатку одной из трех аминокислот, которые имеют гидроксильные группы. Протеинкиназы оказывают значительный эффект на жизнедеятельность клетки, и их активность тщательно регулируется фосфорилированием (в том числе и самофосфорилированием), связыванием с белками-активаторами или белками-ингибиторами и малыми молекулами.
Протеинкиназы регулируют клеточный цикл, рост и дифференцировку клеток, апоптоз. Нарушения работы протеинкиназ приводят к различным патологиям, в том числе, к возникновению некоторых видов рака.[2][3] Для лечения опухолей такой этиологии разрабатывают лекарства, ингибирующие специфические протеинкиназы.[4]
Протеинкиназы классифицируют по остаткам фосфорилируемых аминокислот. Выделяют протеинкиназы, специфичные к остаткам серина и треонина; тирозина; протеинкиназы двойной специфичности (фосфорилирующие остатки трех аминокислот); а также гистидин-специфичные протеинкиназы прокариот.
Тирозиновые протеинкиназы
Тирозиновые протеинкиназы — ферменты, которые переносят фосфатную группу от АТФ на остаток аминокислоты тирозина в белке.[5] Большинство тирозиновых киназ имеют сопряженные тирозинфосфатазы. Тирозиновые киназы классифицируют на две группы: цитоплазматические и трансмембранные (связанные с рецептором).[6]
Цитоплазматические протеинкиназы
Геном человека содержит 32 гена цитоплазматических тирозиновых протеинкиназ (КФ 2.7.10.2). Первым изученным геном тирозинкиназы, не связанной с рецептором, был ген из семейства Src, протоонкогенных тирозиновых киназ. Протеинкиназы этого семейства содержатся почти во всех клетках животных. Было показано, что вирус саркомы Рауса[англ.] (RSV) содержит мутантную копию нормального клеточного гена Src. Белки семейства Src регулируют многие процессы в клетке, участвуют в передаче интегрин-зависимых сигналов в клетку, которые побуждают её деление.
Геном ретровирусов (в том числе, вируса саркомы Рауса) может содержать ген v-src (viral-sarcoma), который является онкогеном; этот ген не содержит кода для С-концевого участка, отвечающего за ингибирование фосфорилирования, поэтому фермент — продукт вирусного гена — постоянно активен в клетке, чем отличается от c-src (клеточного гена), который активируется только некоторыми внешними сигналами (например, факторами роста), и является протоонкогеном.[7][8][9][10]
TCR (T-cell receptor, рецептор антигена Т-лимфоцитов), передает сигнал внутрь клетки путём активирования двух белков: Lck и Fyn, относящихся к семейству Src. Этот сигнал приводит к пролиферации Т-лимфоцитов и усилению клеточного иммунитета.
Рецепторы с тирозинкиназной активностью
Геном человека содержит 58 генов рецепторов-тирозинкиназ[11] (КФ 2.7.10.1). Гормоны и факторы роста, которые взаимодействуют на поверхности клетки с рецепторами, обладающими тирозинкиназной активностью, как правило, вызывают рост клеток и стимулируют клеточные деления (например, инсулин, инсулиноподобный фактор роста 1, эпидермальный фактор роста). Рецепторы с тирозинкиназной активностью располагаются на поверхности клеток и связывают полипептидные факторы роста, цитокины и гормоны. Такие рецепторы не только регулируют клеточные процессы, но и играют критическую роль в развитии многих видов рака.[12]
Рецепторы с тирозинкиназной активностью в зависимости от их субстратов фосфорилирования подразделяют на двадцать семейств (эпителиального фактора роста, инсулина, фактора роста тромбоцитов и другие).[11] Инсулиновый рецептор является мультимерным комплексом, однако большинство рецепторов с тирозинкиназной активностью имеют только одну субъединицу. Каждый мономер имеет один трансмембранный домен, состоящий из 25-38 аминокислотных остатков, внеклеточный N-концевой домен и внутриклеточный C-концевой домен. Внеклеточный домен очень крупный и отвечает за связывание эндогенных лигандов-агонистов (факторов роста или гормонов); внутриклеточный участок содержит домены, обладающие киназной активностью. Когда фактор роста или гормон соединяется с внеклеточным доменом рецептора-тирозинкиназы, рецептор димеризуется. Димеризация рецепторов активирует цитоплазматические домены, которые осуществляют самофосфорилирование рецептора по многим аминокислотным остаткам.
Тирозиновые протеинкиназы принимают участие в передаче сигнала в клетке путём фосфорилирования специфических остатков тирозина белков-мишеней.[13] Специфические белки, содержащие SH2-домены или домены связывания фосфотирозина (Src, фосфолипаза Сγ), соединяются с рецептором и фосфорилируются внутриклеточным доменом. Фосфорилирование приводит к активации этих белков и инициирует пути сигнальной трансдукции.[13] Активированные рецепторы могут взаимодействовать и с другими белками, не обладающими каталитическими активностями. Такие адапторные белки (scaffold proteins) связывают рецепторы-тирозинкиназы со следующими этапами сигнальной трансдукции, например, с каскадом МАР-киназ.[14]
Серин/треонин — специфичные протеинкиназы


Серин-треониновые протеинкиназы (КФ 2.7.11.1) фосфорилируют гидроксильную группу в остатках серина или треонина. Активность этих протеинкиназ регулируется несколькими событиями (например, повреждениями ДНК), а также некоторыми химическими сигналами, в том числе, cAMP, cGMP, диацилглицеролом, Ca2+, кальмодулином.[6][15]
Серин/треониновые протеинкиназы фосфорилируют остатки серина или треонина в консенсусных последовательностях, которые образуют фосфоакцепторный сайт. Эта последовательность остатков аминокислот в молекуле субстрата позволяет осуществлять контакт каталитической щели протеинкиназы с фосфорилируемой областью. Эта особенность делает киназу специфичной не к какому-либо определенному субстрату, но к специфичному семейству белков с одинаковыми консенсусными последовательностями. В то время как каталитические домены этих протеинкиназ высококонсервативны, последовательности узнавания отличаются, обуславливая тем самым узнавание разных субстратов.[6]
Киназа фосфорилазы (КФ 2.7.11.19) была открыта Кребсом в 1959 году[16] и является первым описанным ферментом семейства серин/треониновых протеинкиназ. Киназа фосфорилазы превращает неактивную гликогенфосфорилазу В в активную форму гликогенфосфорилазу A, последняя отщепляет от гликогена остатки глюкозо-1-фосфата. Киназа фосфорилазы активируется протеинкиназой А.
Протеинкиназа А
Протеинкиназа А, или цАМФ-зависимая протеинкиназа, (КФ 2.7.11.1) относится к семейству ферментов, активность которых зависит от уровня циклического АМФ (цАМФ) в клетке. Протеинкиназа А является самой изученной из всех протеинкиназ, её функции разнообразны, она участвует в регуляции метаболизма гликогена, липидов и сахаров, её субстратами могут быть другие протеинкиназы или другие метаболические ферменты. Её следует отличать от АМФ-зависимой протеинкиназы, или АМФК, которая играет важную роль в поддержании энергетического баланса клетки и активируется посредством АМФ, а не цАМФ.
Протеинкиназа А участвует в цАМФ-стимулируемой транскрипции генов, которые имеют цАМФ-реактивный элемент в регуляторном участке. Повышение концентрации цАМФ ведет к активации протеинкиназы А, которая в ответ фосфорилирует транскрипционный фактор CREB по остатку серина 133; CREB своим фосфорилированным участком связывает коактиватор транскрипции и стимулирует транскрипцию.
Молекула протеинкиназы А является холоферментом (то есть, требует кофермент для работы) и в неактивном состоянии является тетрамером — состоит из двух регуляторных и двух каталитических субъединиц. Если уровень цАМФ в клетке низкий, то холофермент (тетрамер) остается интактным, и каталитическая активность отсутствует. Активация аденилатциклазы или ингибирование фосфодиэстераз, расщепляющих цАМФ, приводит к возрастанию концентрации цАМФ в клетке; при этом цАМФ связывается с двумя сайтами связывания на регуляторных субъединицах протеинкиназы А, в результате происходят конформационные изменения фермента, в результате которых тетрамер протеинкиназы А диссоциирует на два каталитически активных димера (каждый из димеров состоит из одной каталитической и одной регуляторной субъединицы). Открытые активные центры каталитических субъединиц переносят концевой фосфат молекулы АТФ на остатки серина или треонина белков - субстратов протеинкиназы А.
Протеинкиназы А представлены во многих типах клеток и проявляют каталитические активности в отношении разных субстратов, таким образом, активность протеинкиназы А и концентрация цАМФ регулируются во многих биохимических путях. Следует отметить, что действие протеинкиназы А, вызванное фосфорилированием белков-субстратов, как правило, кратковременное, так как протеинфосфатазы, сопряженные с протеинкиназами, быстро дефосфорилируют белки-мишени, ранее фосфорилированные протеинкиназой А.
Гормоны инсулин и глюкагон влияют на работу протеинкиназы А, изменяя уровень цАМФ в клетке по механизму активации рецепторов, связанных с G-белками (инсулин действует через тирозинкиназу) и через аденилатциклазу. Инсулин активирует аденилатциклазу, повышая концентрацию цАМФ; протеинкиназа А фосфорилирует ферменты ацетил-КоА-карбоксилазу и пируватдегидрогеназу, направляя таким образом ацетил-КоА для синтеза липидов; глюкагон имеет противоположный эффект.
Активность протеинкиназы А регулируется и по механизму отрицательной обратной связи. Одним из субстратов, активируемых протеинкиназой А, является фосфодиэстераза, которая превращает цАМФ в АМФ, таким образом, снижая концентрацию цАМФ и ингибируя протеинкиназу А.
Протеинкиназа B (Akt)
Геном человека содержит семейство генов Akt1, Akt2, Akt3. Протеинкиназа Akt1 ингибирует процессы апоптоза, принимает участие в регуляции клеточного цикла, индуцирует синтез белка и поэтому является ключевым белком, регулирующим рост тканей, а также отвечает за развитие мышечной гипертрофии. Поскольку продукт гена Akt1 блокирует апоптоз, повышенный уровень экспрессии Akt1 отмечается во многих опухолях. Первоначально Akt1 был охарактеризован как онкоген в трансформирующем ретровирусе AKT8 в 1990 году.
Продукт гена Akt2 является важной сигнальной молекулой в пути передачи сигнала молекулой инсулина, этот белок требуется для транспорта глюкозы.
Показано, что Akt3 преимущественно экспрессируется в мозге. Мыши, лишенные гена Akt3, имеют маленький мозг. Мыши, нокаутные по гену Akt1, но имеющие ген Akt2 имели меньший размер. Так как уровень глюкозы у таких мышей был в норме, была показана роль Akt1 в процессах роста.[17]
Мыши, нокаутные по гену Akt2, но имеющие Akt1, имели задержки роста и фенотипические проявления инсулин-зависимого диабета. Полученные данные указывали на роль Akt2 в проведении сигнала от инсулинового рецептора.[18]
Регуляция активности Akt осуществляется путём связывания фосфолипидов в мембране. Akt содержит PH-домен (Pleckstrin Homology domain, 120 остатков аминокислот), который высокоаффинно связывает фосфатидилинозитол-трифосфат (PIP3) или фосфатидилинозитол-дифосфат (PIP2). PH-домены выполняют функции заякоривания в мембранах. PIP2 может быть фосфорилирован только PIP3-киназами, и только в случае, когда клетка получила сигнал к росту. PIP3-киназы могут быть активированы рецепторами, связанными с G-белками или рецепторами с тирозинкиназной активностью (например, инсулиновым рецептором). Только после активации PIP3-киназы фосфорилируют PIP2 в PIP3.[19]
После связывания с PIP3 и закрепления в мембране Akt может быть активирована путём фосфорилирования фосфоинозитол-зависимыми киназами (PDK1 и PDK2, mTORC2). PDK1 фосфорилирует Akt по остатку серина в положении 473, mTORC2 стимулирует фосфорилирование PDK1. Активированная Akt далее регулирует фосфорилированием активность многих субстратов. Показано, что Akt может быть активирована и без участия PIP3-киназ.
Соединения, повышающие концентрацию цАМФ, могут активировать Akt через протеинкиназу А. Фосфатазы липидов контролируют концентрацию PIP3, например, супрессор опухолей PTEN (phosphatase and tensin homolog deleted on chromosome ten) работает как фосфатаза, и дефосфорилирует PIP3 в PIP2. Фермент Akt диссоциирует от плазматической мембраны, и его активность значительно падает. Протеинфосфатазы контролируют количество фосфорилированного Akt. Инактивация белка Akt происходит за счёт действия фосфатазы PHLPP (PH domain and leucine rich repeat protein phosphatase), которая дефосфорилирует остаток серина в положении 473.[20]
Akt регулирует многие процессы, направленные на выживание клетки, например, он может фосфорилировать проапоптотический белок BAD (из семейства Bcl-2) по остатку серина 136, что вызывает диссоциацию BAD из Bcl-2/Bcl-X комплекса и приводит к утере белком BAD своей проапоптотической функции. Также Akt активирует транскрипционный фактор NF-κB (nuclear factor-kappa B), и включает транскрипцию генов выживания.
Akt требуется для инсулин-индуцируемой транслокации транспортера глюкозы 4 (GLUT4) в плазматическую мембрану. Киназа-3 гликогенсинтетазы (GSK 3) может быть ингибирована фосфорилированием Akt, что вызывает синтез гликогена.
Akt1 также связан с ростом сосудов и с развитием опухолей. Недостаточность Akt1 у мышей ингибирует физиологический ангиогенез, но усиливает патологический рост сосудов и опухолей.[21]
Протеинкиназа С
Протеинкиназы С (PKC, КФ 2.7.11.13) — это семейство протеинкиназ, содержащее порядка десяти изоферментов, которые классифицируют по вторичным посредникам на три семейства: традиционные, или классические (англ. conventional), оригинальные (англ. novel), или нестандартные и атипичные (англ. atypical). Для активации традиционных протеинкиназ С требуется наличие ионов Ca2+, диацилглицерола или фосфатидилхолина. Оригинальные протеинкиназы С активируются молекулами диацилглицерола и не требуют наличия Ca2+. И традиционные, и оригинальные протеинкиназы С активируются через сходные пути сигнальной трансдукции, например, с помощью фосфолипазы С. Атипичные изоформыпротеинкиназы С для активации не требуют ни Ca2+, ни диацилглицерола.
Все ферменты семейства протеинкиназ С состоят из регуляторного и каталитического доменов, связанных шарнирной областью. Каталитические районы высоко консервативны между разными изоформами и значительно отличаются от каталитических районов других серин-треониновых протеинкиназ. Консервативность каталитических доменов связана с выполняемыми функциями; различия в регуляторных районах протеинкиназ С обуславливают различия во вторичных посредниках.
Регуляторный домен протеинкиназы С содержит на N-конце отдельные участки. Домен С1, представленный во всех изоформах протеинкиназы С, имеет сайт связывания диацилглицерола. Домен С2 воспринимает ион Ca2+. Район псевдосвязывания субстрата представляет собой короткую последовательность аминокислот, которые подражают субстрату и занимают участок связывания субстрата в активном центре, делая фермент неактивным.
Ионы Ca2+ связываются с доменом С2, а диацилглицерол (DAG) - с доменом С1; эти лиганды вызывают прикрепление протеинкиназы С к плазматической мембране, что приводит к освобождению псевдосубстрата из каталитического центра и к активации фермента. Для осуществления подобных аллостерических взаимодействий требуется, чтобы каталитический домен протеинкиназы С был предварительно фосфорилирован.
Протеинкиназа С также должна быть предварительно фосфорилирована и для осуществления собственной киназной активности. Молекула протеинкиназы С содержит несколько сайтов фосфорилирования 3-фосфоинозитол-зависимой протеинкиназой-1 (PDK1). Активированная протеинкиназа С переносится к плазматической мембране и присоединяются к RACK-белкам (англ. Receptor for Activated C-Kinase), аминокислотная последовательность которых на 47 % гомологична бета-субъединицам G-белков.
Для протеинкиназ С характерен длительный период активности, которая сохраняется, даже если первоначальный сигнал пропал или снизилась концентрация ионов Ca2+. Это достигается образованием диацилглицерола из фосфатидилхолина с помощью фосфолипазы С.
Последовательность остатков аминокислот в молекуле протеинкиназы С сходна с таковой для протеинкиназы А, и протеинкиназа С содержит остатки основных аминокислот вблизи остатков серина и треонина, подвергающихся фосфорилированию. Субстратами протеинкиназы С являются следующие белки: MAP-киназы, Raf-киназы, MARCKS (англ. myristoylated alanine-rich C-kinase substrate, производные миристоленовой кислоты, богатые аланином, субстраты протеинкиназы С). Белки-субстраты протеинкиназы С играют важную роль в поддержании формы клеток, способности к движению, секреции, трансмембранном транспорте, регуляции клеточного цикла. MARCKS вовлечены в процессы экзоцитоза некоторых секреторных пузырьков, содержащих, муцин и хромафин. MARCKS — кислые белки, содержат большое количество остатков аланина, глицина, пролина и глутаминовой кислоты. MARCKS связаны N-концом с липидами мембраны (через миристоленовую кислоту), регулируются ионами Ca2+, кальмодулином, протеинкиназой С.
VDR (Vitamin D receptor) — кальцитриоловый рецептор. Рецептор стероидных гормонов из семейства ядерных рецепторов. После активирования молекулой витамина D, образует гетеродимер с ретиноидным-Х-рецептором и связывается с регуляторными элементами на ДНК, изменяя экспрессию генов или снимая репрессоры генов. Глюкокортикоиды снижают экспрессию VDR во всех тканях.
Рецептор эпидермального фактора роста (EGFR) — относится к семейству рецепторов факторов роста, связывающих внеклеточные белковые лиганды и обладает тирозинкиназными активностями. Мутации, затрагивающие EGRF часто могут проявляться в раковом перерождении клетки. После связывания лиганда, рецептор димеризуется, происходит самофосфорилирование по пяти остаткам тирозина на С-конце рецептора, и EGRF приобретает внутриклеточную тирозинкиназную активность.[22]
Последующая активность EGRF связана с инициацией каскада сигнальной трансдукции, активируются MAPK, Akt, JNK — что приводит к синтезу ДНК и пролиферации. Киназный домен также может фосфорилировать другие рецепторы, связанные с EGRF по остаткам тирозина.
Ca2+/кальмодулин — зависимые протеинкиназы
Са2+/кальмодулин-зависимые киназы, или СаМ киназы, (КФ 2.7.11.17) регулируются Са2+/кальмодулиновым комплексом. СаМ киназы классифицируют на два класса: специализированные СаМ киназы (например, киназа легких цепей миозина, которая фосфорилирует молекулы миозина, вызывая мышечное сокращение) и многофункциональные СаМ киназы (играют роль во многих процессах: секреции нейромедиаторов, регуляции транскрипционных факторов, в метаболизме гликогена), порядка 2 % белков головного мозга представлены СаМ второго типа.[23]
Кальмодулин (СаМ) — это вездесущий, кальций-связывающий белок, который связывается с многими другими белками и регулирует их активность. Это маленький кислый белок, состоит из 148 аминокислотных остатков, содержит четыре домена связывания кальция.[24]
СаМ служит промежуточным звеном в воспалении, апоптозе, мышечных сокращениях, развитии кратковременной и длительной памяти, росте нервов и иммунном ответе. Кальмодулин экспрессируется во многих типах клеток и находится в цитоплазме, внутри органелл, а также находится в плазматической мембране и мембранах органелл.[25] Многие белки, которые связываются с кальмодулином, не могут сами связывать кальций и используют кальмодулин как «датчик» кальция и компонент системы передачи сигнала.

Кальмодулин также используется для запасания Ca2+ в эндоплазматическом и саркоплазматическом ретикулумах. После связывания кальция молекула кальмодулина претерпевает конформационные изменения, что позволяет молекуле связывать другие белки для осуществления специфического ответа. Молекула кальмодулина может связать до четырёх ионов кальция, может подвергаться посттрансляционной модификации, например, фосфорилированию, ацетилированию, метилированию, протеолизу, причем эти модификации могут модулировать активность СаМ.
Киназа легких цепей миозина. Киназа легких цепей миозина (MLCK) фосфорилирует миозин. Киназа легких цепей миозина имеет ключевое значение в сокращении гладкой мускулатуры.[26] Сокращение гладких мышц может произойти после повышения концентрации кальция в результате притока из саркоплазматического ретикулюма или из внеклеточного пространства. Сперва кальций связывается с кальмодулином, это связывание активирует киназу легких цепей миозина, которая фосфорилирует легкие цепи молекул миозина. Фосфорилирование позволяет молекулам миозина образовывать поперечные мостики и связываться с актиновыми филаментами и стимулирует мышечное сокращение. Данный путь является основным в механизме сокращения гладких мышц, так как гладкие мышцы не содержат тропонинового комплекса, в отличие от поперечно-полосатых.
МАРK (митоген-активируемые киназы)
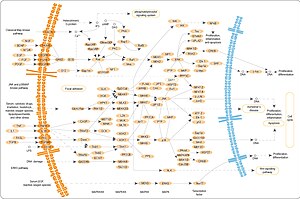
Митоген-активируемые киназы (КФ 2.7.11.24) отвечают на внеклеточные стимулы (митогены) и регулируют многие клеточные процессы (экспрессию генов, деление, дифференцировку и апоптоз). МАРК вовлечены в работу многих неядерных белков — продуктов онкогенов. Внеклеточные стимулы ведут к активации МАРК через сигнальный каскад, который состоит из МАРК, МАРКК (МАР2К) и МАРККК (МАР3К). МАР3К активируется внеклеточными стимулами и фосфорилирует МАР2К, затем МАР2К фосфорилированием активирует МАРК. Такой сигнальный МАРK-каскад консервативен для эукариот от дрожжей до млекопитающих.
MAPK/ERK-киназы принимают участие в особом пути сигнальной трансдукции. ERK — или классические МАР-киназы, регулируются внеклеточными сигналами.[27]
Рецепторы, связанные с тирозиновыми киназами (например, EGFR), активируются внеклеточными лигандами. Связывание EGF с рецептором приводит к фосфорилированию EGFR. Белок GRB2, содержащий SH2-домен, связывается с остатками фосфорилированного тирозина. Белок GRB2 своим SH3-доменом связывается и активирует SOS (гуанин-нуклеотид заменяющим фактором). Активированный гуанин-нуклеотид заменяющий фактор отщепляет ГДФ от белка Ras,[28] Ras далее может связать ГТФ и активироваться.
Активный Ras активирует RAF-киназу (серин-треониновой специфичности). RAF-киназа фосфорилирует и активирует МЕК, другую серин-треониновую киназу. МЕК фосфорилирует и активирует МАРК. Эта серия киназ от RAF к МЕК и к МАРК является примером каскада протеинкиназ.[29]
Один из эффектов активации МАРК это изменение трансляции мРНК. МАРК фосфорилирует и активирует S6 киназу 40S рибосомных белков (RSK). RSK фосфорилирует рибосомный белок S6, и вызывает его диссоциацию от рибосомы.
МАРК регулирует активности нескольких транскрипционных факторов, например, C-myc. МАРК регулирует активность генов, контролирующих клеточный цикл.[27]
Гистидин — специфичные протеинкиназы
Гистидиновые киназы найдены в прокариотах и по своей структуре отличаются от других известных протеинкиназ.[30] У прокариот гистидин-специфичные протеинкиназы работают как часть двухкомпонентной системы сигнальной трансдукции. В ходе фосфорилирования неорганический фосфат отщепляется от АТФ и присоединяется к собственному остатку гистидина, а затем переносится на остаток аспартата белка-мишени. Фосфорилирование аспартата приводит к дальнейшей передаче сигнала.
Гистидиновые киназы широко распространены среди прокариот, растений и грибов. Фермент пируватдегидрогеназа животных, относящийся к семейству протеинкиназ, структурно повторяет гистидиновые киназы, но фосфорилирует остатки серина, и, возможно, не использует гистидин-фосфатный интермедиат.[30]
См. также
Примечания
- ↑ Stout T. J., Foster P. G., Matthews D. J. High-throughput structural biology in drug discovery: protein kinases (англ.) // Curr. Pharm. Des.[англ.] : journal. — 2004. — Vol. 10, no. 10. — P. 1069—1082. — PMID 15078142. Архивировано 9 декабря 2012 года.
- ↑ Capra M., Nuciforo P. G., Confalonieri S., Quarto M., Bianchi M., Nebuloni M., Boldorini R., Pallotti F., Viale G., Gishizky M. L., Draetta G. F., Di Fiore P. P. Frequent alterations in the expression of serine/threonine kinases in human cancers. (англ.) // Cancer research. — 2006. — Vol. 66, no. 16. — P. 8147—8154. — doi:10.1158/0008-5472.CAN-05-3489. — PMID 16912193.
- ↑ Clark D. E., Errington T. M., Smith J. A., Frierson H. F. Jr., Weber M. J., Lannigan D. A. The serine/threonine protein kinase, p90 ribosomal S6 kinase, is an important regulator of prostate cancer cell proliferation. (англ.) // Cancer research. — 2005. — Vol. 65, no. 8. — P. 3108—3116. — doi:10.1158/0008-5472.CAN-04-3151. — PMID 15833840.
- ↑ Zhao Y., Thomas H. D., Batey M. A., et al. Preclinical evaluation of a potent novel DNA-dependent protein kinase inhibitor NU7441 (англ.) // Cancer Research[англ.] : journal. — American Association for Cancer Research[англ.], 2006. — May (vol. 66, no. 10). — P. 5354—5362. — doi:10.1158/0008-5472.CAN-05-4275. — PMID 16707462.
- ↑ Weinberg, Robert A. The Biology Of Cancer. — New York: Garland Science, Taylor & Francis Group, LLC. — С. 757—759. — ISBN 0-8153-4076-1.
- ↑ 1 2 3 Cox, Michael; Nelson, David R. Lehninger: Principles of Biochemistry. — fifth. — W H Freeman & Co, 2008. — ISBN 1-4292-2416-9.
- ↑ Cance W. G., Craven R. J., Bergman M., Xu L., Alitalo K., Liu E. T. Rak, a novel nuclear tyrosine kinase expressed in epithelial cells (англ.) // Cell Growth Differ.[англ.] : journal. — 1994. — December (vol. 5, no. 12). — P. 1347—1355. — PMID 7696183.
- ↑ Lee J., Wang Z., Luoh S. M., Wood W. I., Scadden D. T. Cloning of FRK, a novel human intracellular SRC-like tyrosine kinase-encoding gene (англ.) // Gene[англ.] : journal. — Elsevier, 1994. — January (vol. 138, no. 1—2). — P. 247—251. — doi:10.1016/0378-1119(94)90817-6. — PMID 7510261.
- ↑ Oberg-Welsh C., Welsh M. Cloning of BSK, a murine FRK homologue with a specific pattern of tissue distribution (англ.) // Gene[англ.] : journal. — Elsevier, 1995. — January (vol. 152, no. 2). — P. 239—242. — doi:10.1016/0378-1119(94)00718-8. — PMID 7835707.
- ↑ Thuveson M., Albrecht D., Zürcher G., Andres A. C., Ziemiecki A. iyk, a novel intracellular protein tyrosine kinase differentially expressed in the mouse mammary gland and intestine (англ.) // Biochem. Biophys. Res. Commun.[англ.] : journal. — 1995. — April (vol. 209, no. 2). — P. 582—589. — doi:10.1006/bbrc.1995.1540. — PMID 7733928.
- ↑ 1 2 Robinson D. R., Wu Y. M., Lin SF. The protein tyrosine kinase family of the human genome (англ.) // Oncogene : journal. — 2000. — Vol. 19, no. 49. — P. 5548—5557. — doi:10.1038/sj.onc.1203957. — PMID 11114734.
- ↑ Zwick, E. Bange, J. Ullrich, A. Receptor tyrosine kinase signalling as a target for cancer intervention strategies (англ.) // Endocr. Relat. Cancer[англ.] : journal. — 2001. — Vol. 8, no. 3. — P. 161—173. — doi:10.1677/erc.0.0080161. — PMID 11566607.
- ↑ 1 2 Pawson, T. Protein modules and signalling networks (англ.) // Nature. — 1995. — Vol. 373, no. 6515. — P. 573—580. — doi:10.1038/373573a0. — PMID 7531822.
- ↑ Avruch J., Khokhlatchev A., Kyriakis J. M., et al. Ras activation of the Raf kinase: tyrosine kinase recruitment of the MAP kinase cascade (англ.) // Recent Progress in Hormone Research : journal. — 2001. — Vol. 56, no. 1. — P. 127—155. — doi:10.1210/rp.56.1.127. — PMID 11237210. Архивировано 14 апреля 2013 года.. — «.».
- ↑ Walter F., PhD. Boron. Medical Physiology: A Cellular And Molecular Approach (англ.). — Elsevier/Saunders[англ.], 2005. — ISBN 1-4160-2328-3.
- ↑ Edwin G. Krebs , David S. Love , Gloria E. Bratvold , Kenneth A. Trayser , William L. Meyer , Edmond H. Fischer. Purification and Properties of Rabbit Skeletal Muscle Phosphorylase b Kinase // Biochemistry. — 1964. — Т. 3, вып. 8. — С. 1022—1033. — doi:10.1021/bi00896a003.
- ↑ Easton RM, Cho H, Roovers K, Shineman DW, Mizrahi M, Forman MS, Lee VM, Szabolcs M, de Jong R, Oltersdorf T, Ludwig T, Efstratiadis A, Birnbaum MJ. Role for Akt3/protein kinase Bgamma in attainment of normal brain size // Mol Cell Biol. — 2005. — Т. 25, № 5. — С. 1869—1878. — PMID 15713641.
- ↑ McCurdy CE, Cartee GD. Akt2 is essential for the full effect of calorie restriction on insulin-stimulated glucose uptake in skeletal muscle // Diabetes. — 2005. — Т. 54, № 5. — С. 1349—1356. — PMID 15855319.
- ↑ Северин Е. С. Биохимия. — 5-е. — Гэотар-Медиа, 2008. — 768 с. — ISBN 978-5-9704-0778-3.
- ↑ Brognard J, Sierecki E, Gao T, Newton AC. PHLPP and a second isoform, PHLPP2, differentially attenuate the amplitude of Akt signaling by regulating distinct Akt isoforms // Mol Cell. — 2007. — Т. 25, № 6. — С. 917—931. — PMID 17386267.
- ↑ Qiao M, Sheng S, Pardee AB. Metastasis and AKT activation // Cell Cycle. — 2008. — Т. 7, № 19. — С. 2991—2996. — PMID 18818526.
- ↑ Carpenter G. The EGF receptor: a nexus for trafficking and signaling. (англ.) // BioEssays : news and reviews in molecular, cellular and developmental biology. — 2000. — Vol. 22, no. 8. — P. 697—707. — doi:10.1002/1521-1878(200008)22:8<697::AID-BIES3>3.0.CO;2-1. — PMID 10918300.
- ↑ Manning G., Whyte D. B., Martinez R., Hunter T., Sudarsanam S. The protein kinase complement of the human genome (англ.) // Science : journal. — 2002. — December (vol. 298, no. 5600). — P. 1912—1934. — doi:10.1126/science.1075762. — PMID 12471243.
- ↑ Chin D., Means A. R. Calmodulin: a prototypical calcium sensor (англ.) // Trends Cell Biol.[англ.] : journal. — 2000. — Vol. 10, no. 8. — P. 322—328. — doi:10.1016/S0962-8924(00)01800-6. — PMID 10884684.
- ↑ Stevens F. C. Calmodulin: an introduction (англ.) // Can. J. Biochem. Cell Biol.[англ.] : journal. — 1983. — Vol. 61, no. 8. — P. 906—910. — PMID 6313166.
- ↑ Gao Y., Ye L. H., Kishi H., Okagaki T., Samizo K., Nakamura A., Kohama K. Myosin light chain kinase as a multifunctional regulatory protein of smooth muscle contraction (англ.) // IUBMB Life : journal. — 2001. — June (vol. 51, no. 6). — P. 337—344. — PMID 11758800.
- ↑ 1 2 Pearson G., Robinson F., Beers Gibson T., Xu B. E., Karandikar M., Berman K., Cobb M. H. Mitogen-activated protein (MAP) kinase pathways: regulation and physiological functions (англ.) // Endocrine Reviews[англ.] : journal. — Endocrine Society[англ.], 2001. — Vol. 22, no. 2. — P. 153—183. — doi:10.1210/er.22.2.153. — PMID 11294822.
- ↑ Bonni A., Brunet A., West A. E., Datta S. R., Takasu M. A., Greenberg M. E. Cell survival promoted by the Ras-MAPK signaling pathway by transcription-dependent and -independent mechanisms (англ.) // Science : journal. — 1999. — Vol. 286, no. 5443. — P. 1358—1362. — doi:10.1126/science.286.5443.1358. — PMID 10558990.
- ↑ Hazzalin C. A., Mahadevan L. C. MAPK-regulated transcription: a continuously variable gene switch? (англ.) // Nat. Rev. Mol. Cell Biol. : journal. — 2002. — Vol. 3, no. 1. — P. 30—40. — doi:10.1038/nrm715. — PMID 11823796.
- ↑ 1 2 Besant P. G., Tan E., Attwood P. V. Mammalian protein histidine kinases // Int. J. Biochem. Cell Biol.[англ.]. — 2003. — Март (т. 35, № 3). — С. 297—309. — doi:10.1016/S1357-2725(02)00257-1. — PMID 12531242. Архивировано 31 августа 2017 года.
Литература
- Северин Е. С. Биохимия. — 5-е. — Гэотар-Медиа, 2008. — 768 с. — ISBN 978-5-9704-0778-3.
- Gomperts, Tatham, Kramer. Signal transduction. — London: Elsevier Science, 2003. — 424 с. — ISBN 01-12-289631-9.
- Gerhard Krauss. Biochemistry of Signal Transduction and Regulation. — Second edition. — Germany: Wiley-VCH Verlag GmbH, 2001. — 495 с. — ISBN 3-527-30378-2.
Ссылки
- The Protein Kinase Resource (недоступная ссылка) База данных по структуре протеинкиназ
- Kinase.сom Геномный, эволюционный анализ протеинкиназ
- Kinase3D трехмерные модели протеинкиназ
- Ингибиторы протеинкиназ в развитии
- Подборка последовательностей Ser/Thr/Tyr специфичных протеинкиназ и сходных последовательностей
- Реестр мутаций в белковых доменах протеинкиназ, которые вызывают заболевания
- Статья о киноме человека
- Метод microarray для определения субстратной специфичности протеинкиназ
Эта статья входит в число хороших статей русскоязычного раздела Википедии. |








