Реакция Принса
Реакция Принса (реакция Кривица — Принса) — реакция электрофильного присоединения альдегидов (чаще всего - формальдегида) или кетонов к алкенам с последующим присоединением нуклеофила к образовавшемуся карбокатиону.
Реакция впервые осуществлена Кривицем в 1899г. и детально изучена в 1917 г. Принсом на примере присоединения формальдегида к стиролам с образованием замещенных 1,3,-диоксанов и 1,3-диолов[1].
В зависимости от условий проведения реакции и соотношения компонентов реакция Принса может вести к образованию различных продуктов (в том числе алкенов, образующихся при дегидратации диолов) и их смесей:
Механизм реакции
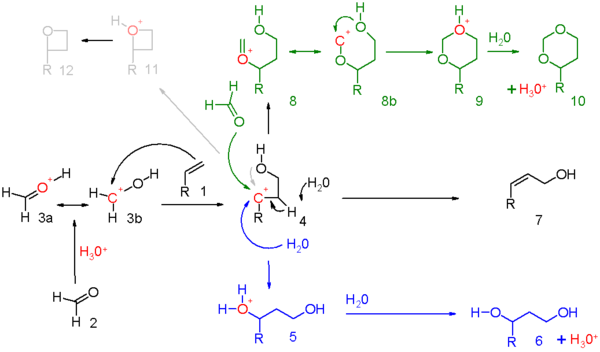
Реакция проходит по механизму электрофильного присоединения карбокатиона 3b, образующегося при протонировании карбонильного компонента 2 к алкену 1, при этом образуется промежуточный карбокатион 4.
Сам Принс первоначально предполагал, что карбокатион циклизуется через ион 11 с образованием оксетана 12, который далее вступает в реакции с формальдегидом или с водой, однако это предположение не подтвердилось.
Карбокатион 4 в условиях реакции может:
- Реагировать с избытком карбонильного соединения, образуя 1,3-диоксаны 10 (показано зеленым);
- Отщеплять протон с образованием аллиловых спиртов 7 (показано черным);
- Присоединять воду с образованием 1,3-диолов 6 (показано синим).
Классическая реакция Принса
В классическом варианте реакции в качестве карбонильного компонента используется формальдегид 2 и основным продуктом реакции являются 1,3-диолы 3, реакция проводится в ледяной уксусной кислоте при катализе серной кислотой[1], именно в этом варианте она описана наиболее широко.
Вместе с тем, в зависимости от условий проведения реакции образующиеся 1,3-диолы 3 могут подвергаться дальнейшим превращениям, наиболее частыми из них являются образование с избытком формальдегида циклических ацеталей - 1,3-диоксанов 5 и дегидратация с образованием аллиловых спиртов 4:
Так, реакция стирола с избытком формальдегида в присутствии серной кислоты ведет к образованию 4-фенил-1,3,-диоксана с выходом ~80%, замещенные стиролы в этих условиях также образуют соответствующие 1,3,-диоксаны 5 с выходами 58-96%[2].
При проведении реакции в уксусной кислоте образующиеся гликоли или продукты их дегидратации - аллиловые спирты - могут ацилироваться с образованием соответствующих ацетильных производных[3].
В дальнейшем было показано, что в реакцию вступают, кроме формальдегида, и другие карбонильные соединения с повышенной электрофильностью углерода карбонильной группы - в частности, хлораль и перфторкетоны.
Применение
В промышленности реакция Принса используется для синтеза 1,3-диолов, одним из применений этой реакции является промышленный синтез изопрена, использующегося для синтеза каучуков из изобутилена и формальдегида:
Примечания
- ↑ 1 2 Prins, H J (1919). "On the Condensation of formaldehyde with some unsaturated compounds" (PDF). Proceedings of Royal Netherlands Academy of Arts and Sciences. 22 (I): 51—56. Архивировано (PDF) 20 октября 2020. Дата обращения: 19 октября 2020.
- ↑ Shriner, R.L.; Ruby, Philip R. (1953). "4-PHENYL-m-DIOXANE". Organic Syntheses. 33: 72. doi:10.15227/orgsyn.033.0072. eISSN 2333-3553. ISSN 0078-6209. Архивировано 19 октября 2020. Дата обращения: 19 октября 2020.
- ↑ Price, Charles C.; Benton, F. Lee.; Schmidle, Claude J. (1949-08). "The Preparation of Some 2-Aryl-1,3-butadienes". Journal of the American Chemical Society. 71 (8): 2860—2862. doi:10.1021/ja01176a081. eISSN 1520-5126. ISSN 0002-7863. Архивировано 20 октября 2020. Дата обращения: 19 октября 2020.